El dolor crónico sigue siendo uno de los mayores desafíos de la medicina moderna, a pesar de los grandes avances tecnológicos. En este contexto, la ciencia explora alternativas cada vez más sofisticadas y singulares, siendo una de ellas la estimulación auricular transcutánea del nervio vago (taVNS, por sus siglas en inglés).
¿Podemos, mediante impulsos eléctricos apenas perceptibles en la piel del oído, modular redes cerebrales implicadas en el dolor y la inflamación? Lejos de ser magia, esta propuesta tiene una base neurofisiológica sólida, aunque no exenta de interrogantes.
La estimulación del oído con fines terapéuticos tiene raíces históricas que se extienden a través de diversas culturas y civilizaciones. Los textos más antiguos conocidos sobre medicina china y acupuntura ya mencionaban la estimulación táctil del meato auditivo. Pero no sólo se limitó a China, miles de años atrás, en Arabia, era común la práctica de cauterizar una porción del pabellón auditivo en ciertas tribus, mientras que, en el Antiguo Egipto, las mujeres se lo perforaban o cauterizaban con fines anti-nociceptivos, y los médicos de la antigua Persia trataban el dolor ciático y las enfermedades de transmisión sexual mediante la cauterización auricular.
En lo que respecta a la medicina occidental, el anatomista y cirujano italiano Antonio Vasalva describió el tratamiento del dolor de muelas mediante la escarificación del antitrago de la oreja, en su obra “Tractatus de Aure Humana” (1794). Ya en la segunda mitad del siglo XX, la acupuntura auricular, es decir, la punción con agujas de áreas específicas del pabellón auditivo, ganó popularidad en la medicina clínica de la mano de la obra de Paul Nogier en 1957. Esto dio lugar a la evaluación de la somatotopía auricular, la cual estableció un mapa de puntos de acupuntura, así como al desarrollo de la acupuntura auricular como un “microsistema” dentro del concepto general de acupuntura, sobre cuya aplicación hay revisiones sistemáticas publicadas acerca de sus beneficios en el tratamiento del insomnio, incluso en el alivio del dolor agudo y crónico. De hecho, el concepto de la estimulación transcutánea del nervio vago (tVNS, por sus siglas en inglés) surge de la convergencia de la “neuromodulación” moderna y dicha tradición de estimulación auricular.
Aunque el enfoque de estimulación del oído es ancestral, la estimulación del nervio vago (VNS, por sus siglas en inglés) como terapia “neuromoduladora eléctrica” tiene sus propios antecedentes. Y es que los orígenes se remontan a más de 100 años, cuando a finales del siglo XVIII y principios del XIX el neurólogo estadounidense James L. Corning desarrolló una “horquilla carotídea”, un dispositivo para facilitar la compresión carotídea, y luego la complementó con electrodos de estimulación. Corning intentaba estimular las ramas cervicales del nervio vago para disminuir la frecuencia cardíaca y, posteriormente, el flujo sanguíneo cerebral. Y aunque fue exitoso, el método no fue ampliamente aceptado debido a problemas de seguridad y a la falta de reproducibilidad de la respuesta terapéutica.
Entonces, la VNS implantable (iVNS, por sus siglas en inglés) fue desarrollada en la década de 1980, y aprobada por la Food and Drug Administration (FDA), de Estados Unidos, en 1997 para la epilepsia y en 2005 para la depresión, ambas farmacorresistentes. Posteriormente, las técnicas no invasivas, como la taVNS (estimulación auricular transcutánea) y la tcVNS (estimulación cervical transcutánea), surgieron como alternativas más económicas, menos agresivas y más amigables para el paciente, aprovechando la distribución cutánea de las fibras vagales en la oreja o el cuello.
La taVNS, por lo tanto, es una síntesis moderna de la sabiduría terapéutica auricular de la historia y la tecnología de neuromodulación desarrollada a partir del éxito de la iVNS, dirigida específicamente a la rama auricular del nervio vago (ABVN, por sus siglas en inglés). Hoy en día, hay dispositivos de taVNS frecuentemente utilizados que han recibido certificación europea (CE, que indica conformidad legal y seguridad, pero no necesariamente eficacia clínica) para la epilepsia y depresión desde 2010, para el dolor crónico desde 2012, y para la ansiedad desde 2019.
La taVNS aprovecha una característica anatómica singular, y es que la ABVN inerva zonas concretas del pabellón auditivo, especialmente la concha auricular y el trago interno. No obstante, conviene tener en cuenta que la inervación de la oreja no pertenece exclusivamente al nervio vago, recibiendo también fibras del trigémino y del facial, así como de nervios cervicales. Esto explica por qué la localización exacta de los electrodos podría ser relevante y por qué resulta tan difícil establecer en los estudios una zona de estimulación control o “Sham”. De hecho, el lóbulo de la oreja se ha usado comúnmente como control porque se cree que carece de aferentes vagales, pero su estimulación no es “fisiológicamente inerte” y puede producir patrones de activación en resonancia magnética funcional (fMRI, por sus siglas en inglés) similares a los que se activan con la estimulación de la ABVN, y efectos analgésicos propios.
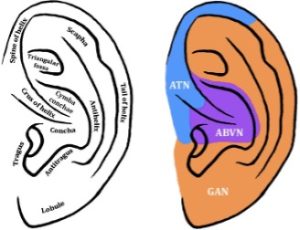
Diagrama del oído externo y su hipotética inervación cutánea. Tomada de: Butt et al., 2020. Figura 1. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC7083568/
ATN: nervio auriculotemporal; GAN: nervio auricular mayor; ABVN: rama auricular del nervio vago
En definitiva, aplicando un estímulo eléctrico en el oído externo se buscan activar las fibras aferentes del nervio vago, las cuáles hipotéticamente transmitirían la señal hasta el núcleo del tracto solitario (NTS), el principal centro de relevo para la información vagal en el tronco encefálico. La “cascada” neurofisiológica que se esperaría tras la activación del NTS sería la estimulación del Locus Coeruleus (LC), que resultaría en una producción de norepinefrina (NE), que a su vez estimularía el Núcleo Dorsal del Rafe (DRN, por sus siglas en inglés) para liberar serotonina (5-HT), y todo ello se asociaría con una mayor plasticidad sináptica y neurogénesis.
La estimulación del NTS podría, por tanto, influir directamente en una red de áreas cerebrales implicadas en el control del dolor, como lo son los propios núcleos LC y DRN, así como la Sustancia Gris Periacueductal (PAG, por sus siglas en inglés). Estas estructuras podríamos decir que son los “centros de mando” de las llamadas vías descendentes inhibitorias del dolor, las cuáles atenúan la transmisión de la información nociceptiva desde la médula espinal. Diversos estudios apuntan a que la taVNS podría reforzar dichas vías descendentes y reducir la percepción subjetiva del dolor. Por ejemplo, en un ensayo piloto en pacientes con artrosis de rodilla, una sola sesión de taVNS mejoró la modulación condicionada del dolor (CPM), una medida indirecta de la capacidad endógena del sistema nervioso para filtrar estímulos dolorosos.
En la literatura también se sugiere que la taVNS podría modular redes neuronales clave que participan no sólo en la gestión del dolor, sino también en la regulación del estado emocional y la respuesta autonómica. En pacientes con dolor lumbar crónico se ha observado que la taVNS aumenta la conectividad funcional estática (sFC, por sus siglas en inglés) entre la PAG y la amígdala izquierda, lo cual podría tener un efecto antinociceptivo, pero que a su vez también mejora la sFC entre el Área Tegmental Ventral (VTA, por sus siglas en inglés), parte de la red de recompensa, y el Córtex Cingulado Anterior. Esta última conectividad incrementada podría moldear procesos cognitivos, motivacionales y de recompensa asociados a la experiencia dolorosa.
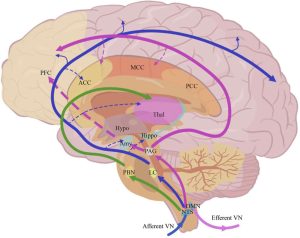
Vías neuronales implicadas en la modulación del dolor mediante la estimulación del nervio vago (VNS, por sus siglas en inglés). Tomada de: Shao et al, 2023. Figura 1. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC10614462/
ACC: corteza cingulada anterior; Amy: amígdala; DMN, núcleo motor dorsal; Hippo, hipocampo; Hypo, hipotálamo; LC, locus coeruleus; MCC, corteza cingulada media; NTS, núcleo del tracto solitario; PAG, sustancia gris periacueductal; PBN, núcleo parabraquial; PCC, corteza cingulada posterior; PFC, corteza prefrontal; Thal, tálamo.
El segundo gran mecanismo hipotético por el cual la taVNS podría mejorar la gestión del dolor es la modulación de la inflamación sistémica, pues el nervio vago ejerce un control directo sobre la respuesta inmunitaria mediante la llamada vía antiinflamatoria colinérgica. Este mecanismo ha sido descrito en enfermedades autoinmunes y podría explicar parte del beneficio observado con la taVNS en patologías dolorosas con componente inflamatorio persistente. En resumen, en esta vía, a través de la liberación de acetilcolina, se activan receptores alfa-7 nicotínicos (α7-nAChR) en macrófagos y otras células inmunes, y esto inhibe la producción de citoquinas proinflamatorias (TNF-α, IL-8 o IL-1β) y favorece la de citoquinas antiinflamatorias (IL-10). Otros mecanismos propuestos por los que la taVNS podría ejercer un efecto antiinflamatorio serían la activación del eje hipotálamo-hipofisario-adrenal (HPA, por sus siglas en inglés), promoviendo la liberación de cortisol, así como la producción de mediadores pro-resolutivos especializados (SPM, por sus siglas en inglés), los cuales se expresan en células inmunitarias, células gliales y neuronas, y actúan sobre sus receptores para modular la inflamación y neuroinflamación.
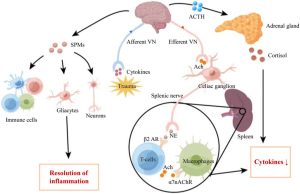
Ilustración esquemática del efecto antiinflamatorio de la estimulación del nervio vago. Tomada de: Shao et al, 2023. Figura 1. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC10614462/
Ach: acetilcolina; ACTH: hormona adrenocorticotropa; NE: norepinefrina; SPMs: mediadores pro-resolutivos especializados; VN: nervio vago; β2 AR: β2 receptor adrenérgico; α7nAChR: α7 receptor nicotínico ACh; HPAA, eje hipotálamo-pituitario-adrenal.
La literatura científica sobre tVNS en dolor es abundante, pero heterogénea. Una revisión sistemática y metaanálisis reciente encontró un efecto global positivo y prometedor, aunque modesto, en la mejoría del dolor crónico, tanto con estimulación auricular como cervical. Sin embargo, la variabilidad entre estudios es muy alta. Así, por ejemplo, en migraña, los resultados son prometedores para la prevención de ataques, especialmente utilizando frecuencias bajas (≈ 1Hz); en la fibromialgia, en cambio, los hallazgos son inconsistentes; en el síndrome del colon irritable, algunos trabajos sugieren ciertos beneficios, pero la evidencia aún es limitada; en dolor lumbar crónico, la taVNS, sola o combinada con otras terapias, produce mejorías en el dolor comparables a la acupuntura o el ejercicio moderado; también hay evidencia de reducción del dolor en otras condiciones dolorosas como la artritis reumatoide y la osteoartritis de rodilla. Pero el principal problema es la falta de estandarización: se usan diferentes dispositivos (a veces incluso TENS convencionales), intensidades, frecuencias, duraciones y puntos de aplicación, lo cual dificulta mucho la comparación de resultados.
Una buena noticia es que la taVNS tiene un excelente perfil de seguridad, siendo los efectos adversos informados leves y transitorios: irritación cutánea, leve molestia o sensación de hormigueo en la oreja. Esto convierte a la taVNS en una opción atractiva para la investigación clínica y potencialmente útil como terapia complementaria no invasiva.
Como grandes retos pendientes, la taVNS todavía enfrenta importantes desafíos científicos:
- El control placebo (Sham), ya mencionado. Esto pone en duda los resultados obtenidos en ensayos clínicos previos.
- La variabilidad individual, pues la densidad de fibras auriculares del vago varía entre personas, lo que podría explicar por qué algunos pacientes responden y otros no.
- La medición de la activación vagal, en la que algunos biomarcadores, como los potenciales evocados somatosensoriales del vago (VSEPs, por sus siglas en inglés), podrían no reflejar la activación real del vago, sino artefactos miogénicos o el resultado de la co-estimulación de otros nervios.
- Protocolos inconsistentes, en los que, sin estandarización de parámetros (frecuencia, intensidad, punto de aplicación, duración, etc.), no es posible definir “la dosis óptima”.
- Falta de estudios a largo plazo, pues la mayoría de los ensayos clínicos son pequeños y de corta duración. Se necesitan estudios de mayor población, controlados y con seguimiento prolongado en el tiempo.
Para concluir, la estimulación transcutánea auricular del nervio vago es una técnica no invasiva, segura y fisiológicamente plausible. Los resultados clínicos actuales son prometedores pero variables, y reflejan un campo aún en evolución. La clave estará en afinar los protocolos, mejorar los modelos experimentales y comprender mejor la interacción fisiológica entre estímulo y respuesta. Las técnicas de neuroimagen funcional podrían ayudar a identificar patrones de conectividad cerebral asociados a una mejor respuesta, y el uso de marcadores neuroquímicos o autonómicos (como la variabilidad de la frecuencia cardiaca o HRV, por sus siglas en inglés) podrían permitir ajustar los parámetros de estimulación en tiempo real. Además, comprender mejor la inervación compleja del pabellón auricular podría abrir la puerta a intervenciones más focalizadas, estimulando de forma selectiva las ramas nerviosas asociadas a diferentes tipos de dolor.
En definitiva, más que magia, la taVNS representa una frontera científica apasionante, donde la neurofisiología y la tecnología se encuentran para replantear el manejo del dolor desde una perspectiva integradora y de precisión.
Juan Montaño Ocaña
Miembro del Grupo de Investigación en el Estudio y Manejo Integral del Dolor de la Universidad Europea
Referencias bibliográficas
- Butt MF, Albusoda A, Farmer AD, Aziz Q. The anatomical basis for transcutaneous auricular vagus nerve stimulation. J Anat. 2020 Apr;236(4):588-611. doi: 10.1111/joa.13122. Epub 2019 Nov 19. PMID: 31742681; PMCID: PMC7083568.
- Farmer AD, Strzelczyk A, Finisguerra A, Gourine AV, Gharabaghi A, Hasan A, Burger AM, Jaramillo AM, Mertens A, Majid A, Verkuil B, Badran BW, Ventura-Bort C, Gaul C, Beste C, Warren CM, Quintana DS, Hämmerer D, Freri E, Frangos E, Tobaldini E, Kaniusas E, Rosenow F, Capone F, Panetsos F, Ackland GL, Kaithwas G, O’Leary GH, Genheimer H, Jacobs HIL, Van Diest I, Schoenen J, Redgrave J, Fang J, Deuchars J, Széles JC, Thayer JF, More K, Vonck K, Steenbergen L, Vianna LC, McTeague LM, Ludwig M, Veldhuizen MG, De Couck M, Casazza M, Keute M, Bikson M, Andreatta M, D’Agostini M, Weymar M, Betts M, Prigge M, Kaess M, Roden M, Thai M, Schuster NM, Montano N, Hansen N, Kroemer NB, Rong P, Fischer R, Howland RH, Sclocco R, Sellaro R, Garcia RG, Bauer S, Gancheva S, Stavrakis S, Kampusch S, Deuchars SA, Wehner S, Laborde S, Usichenko T, Polak T, Zaehle T, Borges U, Teckentrup V, Jandackova VK, Napadow V, Koenig J. International Consensus Based Review and Recommendations for Minimum Reporting Standards in Research on Transcutaneous Vagus Nerve Stimulation (Version 2020). Front Hum Neurosci. 2021 Mar 23;14:568051. doi: 10.3389/fnhum.2020.568051. PMID: 33854421; PMCID: PMC8040977.
- Shao P, Li H, Jiang J, Guan Y, Chen X, Wang Y. Role of Vagus Nerve Stimulation in the Treatment of Chronic Pain. 2023;30(1):167-183. doi: 10.1159/000531626. Epub 2023 Jun 27. PMID: 37369181; PMCID: PMC10614462.
- Chen J, Kuang H, Chen A, Dungan J, Cousin L, Cong X, Patel P, Starkweather A. Transcutaneous Auricular Vagus Nerve Stimulation for Managing Pain: A Scoping Review. Pain Manag Nurs. 2025 Feb;26(1):33-39. doi: 10.1016/j.pmn.2024.11.006. Epub 2024 Dec 16. PMID: 39690039.
- Gerges ANH, Williams EER, Hillier S, Uy J, Hamilton T, Chamberlain S, Hordacre B. Clinical application of transcutaneous auricular vagus nerve stimulation: a scoping review. Disabil Rehabil. 2024 Dec;46(24):5730-5760. doi: 10.1080/09638288.2024.2313123. Epub 2024 Feb 16. PMID: 38362860.
- Costa V, Gianlorenço AC, Andrade MF, Camargo L, Menacho M, Arias Avila M, Pacheco-Barrios K, Choi H, Song JJ, Fregni F. Transcutaneous vagus nerve stimulation effects on chronic pain: systematic review and meta-analysis. Pain Rep. 2024 Aug 7;9(5):e1171. doi: 10.1097/PR9.0000000000001171. PMID: 39131814; PMCID: PMC11309651.
- Li T, Wu Y, Li Y, Hodges SA, Reddy S, Chen L, Sacca V, Kong J. Transcutaneous auricular nerve stimulation modulates the functional connectivity of the descending pain modulation system and reward network in patients with chronic low back pain. Neurotherapeutics. 2025 Sep;22(5):e00611. doi: 10.1016/j.neurot.2025.e00611. Epub 2025 Jun 2. PMID: 40461351; PMCID: PMC12491802.
- Aoyagi K, Rivas E, Shababi R, Edwards R, LaValley M, Lechuga J, Napadow V, Neogi T. Safety and preliminary efficacy of transcutaneous auricular vagus nerve stimulation on chronic knee pain: A pilot trial. Osteoarthr Cartil Open. 2024 Nov 23;7(1):100545. doi: 10.1016/j.ocarto.2024.100545. PMID: 39687279; PMCID: PMC11647485.


